Tel: 0512-66958483
Email: engforlife-mkt@efl-tech.com
自愈合水凝胶凭借动态可逆化学键(如硼酸酯键、氢键、电荷作用)实现受损后快速自主愈合,无需外界触发,可有效弥补传统水凝胶易断裂、寿命短、稳定性差的短板。尤其是在创面愈合、微创给药、骨科修复及柔性生物器件等领域可显著提升材料服役寿命、治疗持久性与修复效果,是一类极具临床转化价值的智能生物材料。
READING
一、水凝胶自愈合:到底测什么?
简单说:断了→拼回去→看能不能复原
评价核心:
(1)宏观能不能长在一起、无缝隙
(2)力学/流变能不能恢复
(3)愈合速度、愈合效率
(4)多次损伤后是否还能愈合
READING
二、水凝胶的自愈合有哪些表征手段
1.宏观直观观察法(最基础、必做)
操作步骤
把水凝胶切成两段(一半染色更明显)
切面贴合,室温/37℃静置一段时间
拍照记录愈合过程,可提拉、弯折验证强度
优点:直观、快速、无设备、文章必放图
缺点:只能定性,不能量化
2.交替阶跃应变流变测试(黄金标准、定量神器)
操作步骤
流变仪设置:交替高低应变
低应变(如1%、5%):凝胶完整,G′高
高应变(如100%–1000%):网络断裂,G′骤降
循环多次,看G′能否快速回弹、无衰减
判断标准
高应变→G′↓(破坏)
低应变→G′迅速复原(自愈合)
多次循环不衰减=优秀自愈合
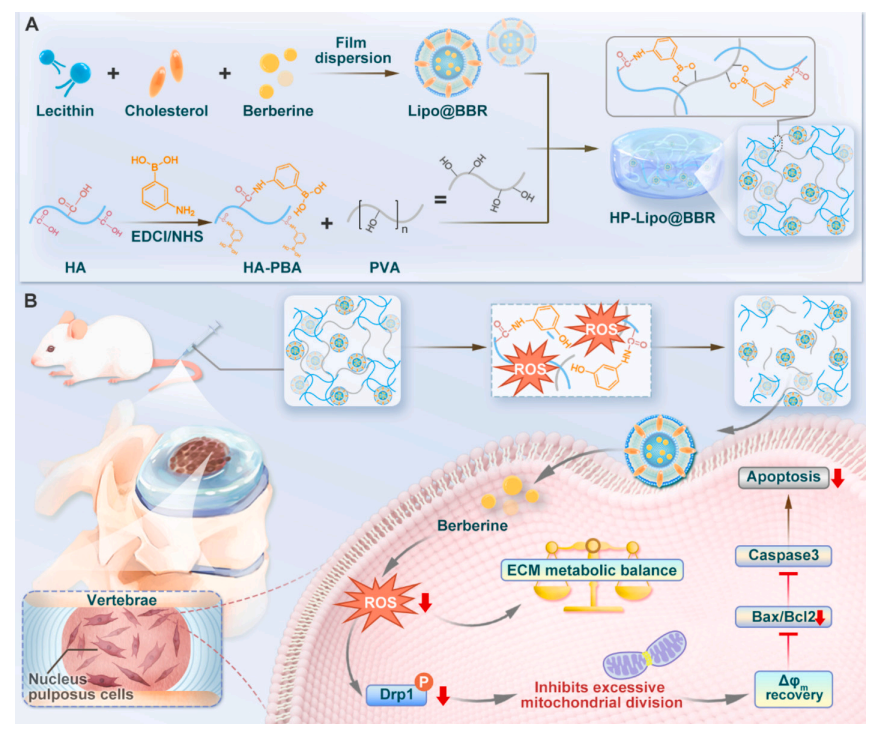
案例一:Chemical Engineering Journal(IF=13.2)负载小檗碱脂质体的ROS响应型水凝胶通过抑制线粒体分裂和细胞凋亡来预防椎间盘退变
参考资料:
https://doi.org/10.1016/j.cej.2025.167108
简介:基于动态硼酸酯键构建ROS响应型水凝胶,负载小檗碱脂质体,通过清除ROS、抑制线粒体分裂与凋亡,实现椎间盘退变的微创靶向修复,兼具自愈合、可注射与生物相容性。
检测手段:
1.交替阶跃应变流变测试
测试条件:应变在5%↔260%之间循环切换
现象:
高应变(260%)→G’骤降(凝胶被破坏)
回到低应变(5%)→G’立即快速恢复
多次循环后模量无明显衰减
结论:证明水凝胶网络被破坏后可快速、重复自愈合
2.宏观自愈合照片
方法:将水凝胶切成两半,界面接触,37℃孵育30min
现象:断裂界面完全融合、连接成整体,拉伸后不断裂
结论:肉眼可见的界面愈合与力学恢复
本研究通过交替阶跃应变流变测试定量证实水凝胶可快速恢复模量,并结合宏观自愈合照片直观证明断裂界面可完全融合,共同证实HP-Lipo@BBR水凝胶具有优异的自愈合性能。
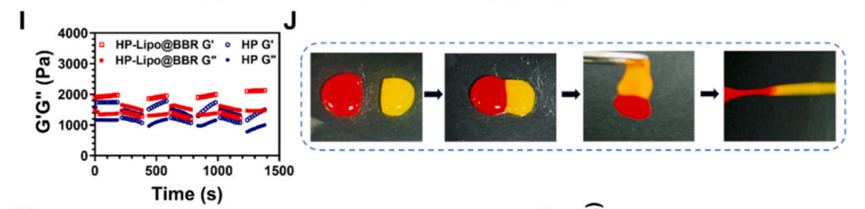
图1 HP-Lipo@BBR水凝胶的交替阶跃应变流变与宏观自愈合性能
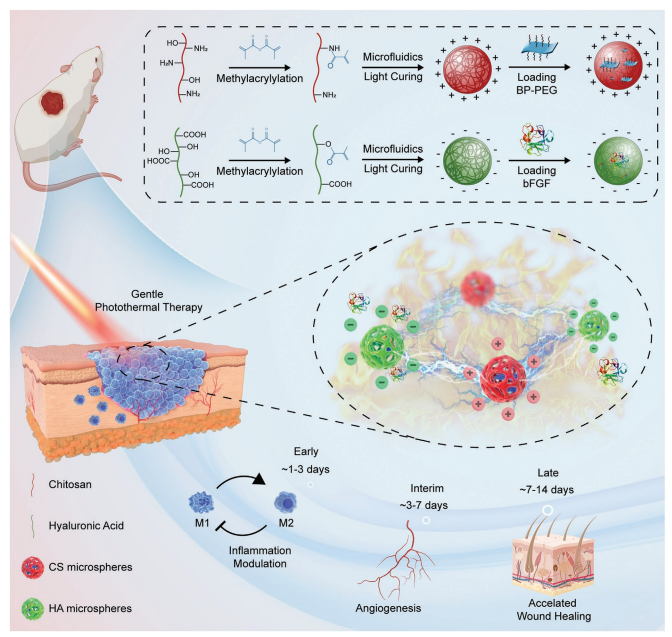
案例二:Advanced Functional Materials(IF=19)用于糖尿病创面联合药物递送与光热治疗的电荷驱动自组装微球水凝胶支架
参考资料:
https://doi.org/10.1002/adfm.202214036
简介:采用正、负电荷微球通过静电自组装构筑微球水凝胶支架,负载黑磷与生长因子,结合光热与药物缓释,实现糖尿病创面抗菌、抗炎、促血管再生与快速愈合。
检测手段:
1.宏观拼接自组装实验
方法:把正电CS微球和负电HA微球各染不同颜色
现象两者接触后无需触发、无需外力,立刻自动拼接成完整整体
结论:依靠静电相互作用,破碎/分离后可自动重新组装愈合。
2.注射器挤出-重塑实验(证明可注射+自愈合)
方法:把混合微球用22G针头挤出
现象:挤出后仍能保持链状结构、不散掉,重新分散到水里依然保持整体结构
结论:剪切破碎后能立刻重新组装,典型的自愈合/可重塑行为。
该电荷驱动微球水凝胶(SMHS)通过宏观双色微球拼接实验与注射器挤出重塑实验,证实其可依靠静电相互作用实现无需外源刺激的快速自组装与自愈合,并具备良好的可注射性与结构稳定性。
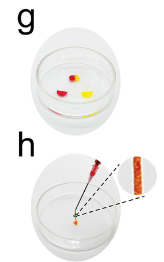
图2 电荷驱动自愈合性能与注射成型性能
视频1 水凝胶通过注射器挤出
视频2 挤出后凝胶的自愈合性能
案例三:Chemical Engineering Journal(IF=13.2)靶向ROS‑衰老‑纤维化轴:一种抗椎间盘退变的双管齐下策略
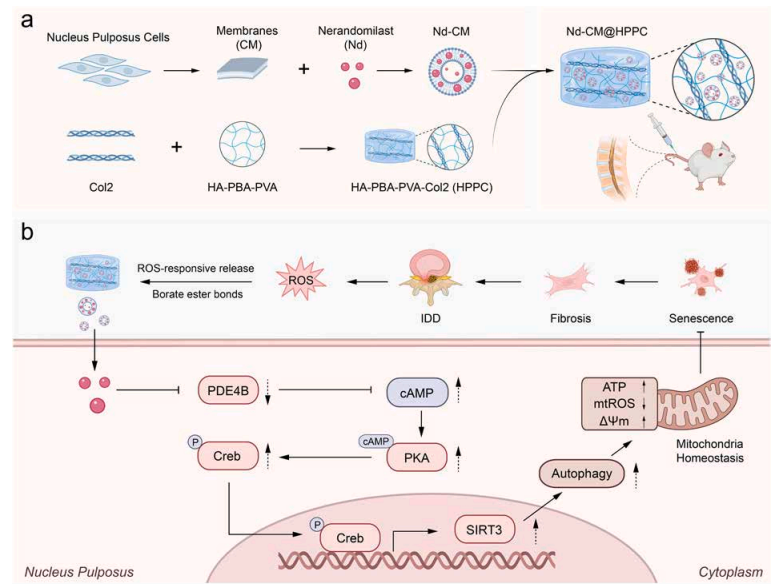
参考资料:
https://doi.org/10.1016/j.cej.2026.174938
简介:针对椎间盘退变“ROS-衰老-纤维化”轴,设计可注射自愈合ROS响应水凝胶,搭载靶向纳米囊泡,双重干预延缓退变、重塑微环境,提升力学与结构修复效果。

图3 自愈合性能验证
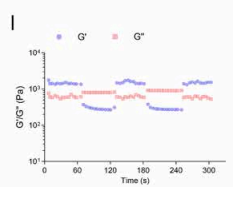
图4 动态应变扫描流变测试
检测手段:
1.宏观自愈合性能
方法:将HPPC水凝胶均匀切割为两半,将两个断面紧密贴合接触,观察并记录宏观愈合状态。
现象:水凝胶切面在无外界刺激、无额外交联条件下,可自动快速愈合并连接为完整一体,界面消失。
结论:该水凝胶具有直观、高效的宏观自愈合能力,依靠动态硼酸酯键可实现断裂后的自主界面愈合与结构恢复。
2.流变自愈合与可恢复性
方法:采用动态应变扫描流变测试,在低应变(1%)与高应变(100%)之间交替循环,监测储能模量G′与损耗模量G″的变化。
现象:低应变下G′>G″,保持稳定凝胶状态;高应变下网络破坏、G′显著下降;回到低应变后G′可迅速恢复至初始水平,多次循环无明显衰减。
结论:HPPC水凝胶具有快速、可逆、可重复的自愈合性能,动态网络在破坏后可快速重建,力学性能完全恢复。
该HPPC水凝胶通过宏观自愈合观察、交替阶跃应变流变测试共同证实其基于动态硼酸酯键的优异自愈合性能、可注射性与结构稳定性。
案例四:ACS Applied Materials & Interfaces(IF=8.2)负载血管内皮生长因子基因工程化内皮细胞外囊泡的活性氧响应型微凝胶:通过微环境重编程实现糖尿病创面愈合
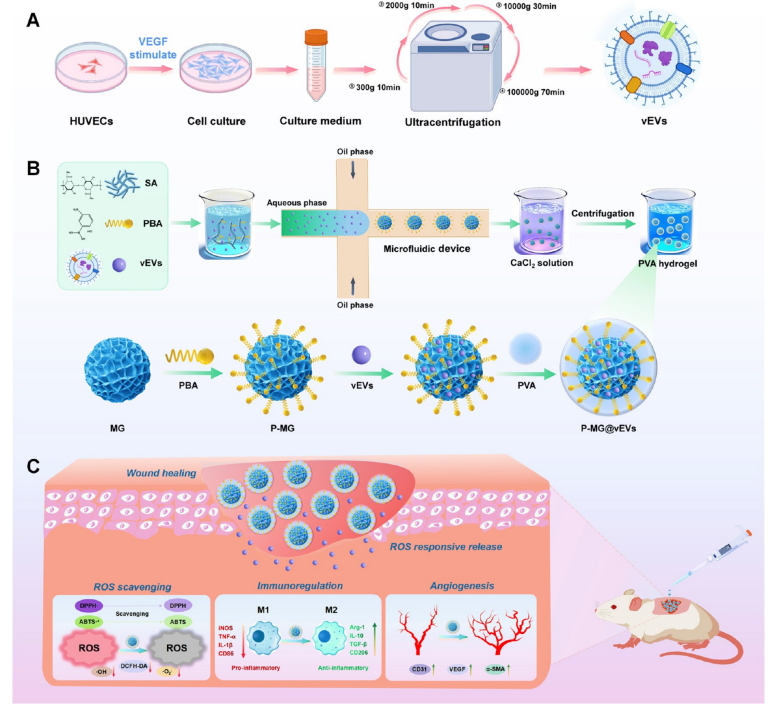
参考资料:
https://doi.org/10.1021/acsami.5c25922
简介:制备ROS响应型微凝胶包裹血管化细胞外囊泡,实现创面抗氧化、调控巨噬细胞极化、促进血管生成,高效改善糖尿病创面微环境并加速愈合。
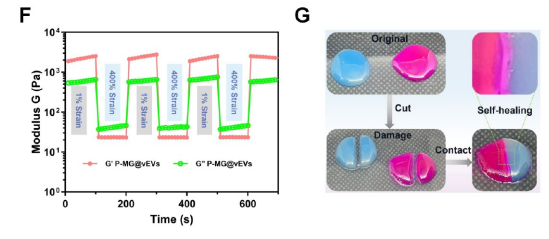
图5 微凝胶的流变自愈合与宏观自愈合性能
检测手段:
1.宏观自愈合
方法:将P‑MG@vEVs微凝胶切成两段,将断面紧密贴合接触,观察宏观愈合情况。
现象:分离的微凝胶片段在接触后可自发重新连接、融合为完整一体,界面消失。
结论:该微凝胶具有直观的宏观自主自愈合能力,断裂后可快速界面愈合。
2.流变自愈合
方法:采用连续阶跃应变流变测试,交替施加低应变(1%)和高应变(400%),记录G′与G″变化。
现象:高应变下凝胶网络破坏,G′明显下降;回到低应变后,G′与G″可瞬间快速恢复,多次循环无明显衰减。
结论:微凝胶在交替阶跃应变流变测试中展现出快速、可逆、可重复的模量恢复能力,具备优异的流变自愈合性能。
微凝胶具备快速、可逆、可重复的流变自愈合性能,动态网络可快速重建。
P‑MG@vEVs微凝胶基于动态硼酸酯键与钙离子配位键,具备快速、自主、可重复的自愈合能力,兼具可注射性与力学稳定性。
方法优缺点对比

综上,以上四篇研究中的水凝胶均依托动态硼酸酯键、静电相互作用、配位作用等可逆键实现了优异的自愈合性能,并通过宏观界面愈合实验与交替阶跃应变流变测试共同验证;自愈合特性赋予材料可注射、剪切变稀、重复抗损伤、结构长效稳定等核心优势,使其能适配微创递送、不规则缺损填充与体内复杂力学环境,为椎间盘退变修复与糖尿病创面愈合提供了稳定、自适应、高生物相容性的智能材料平台,是实现高效组织修复的关键功能基础。
EFL小贴士
愈合好的水凝胶:交替应变G′回弹快、多次不衰减
动态键(硼酸酯、二硫键、希夫碱、氢键)是自愈合关键
一半染色、界面愈合更明显,配图档次直接拉满