Tel: 0512-66958483
Email: engforlife-mkt@efl-tech.com
水凝胶的抗氧化性能,是指能够高效清除体内过量产生的自由基与活性氧(ROS),有效缓解氧化应激损伤,在慢性伤口愈合、抗炎修复、皮肤抗衰、骨组织工程等生物医学领域具备极高的应用潜力。在相关课题研究中,研究者通常选取DPPH、ABTS、PTIO、羟基自由基(·OH)、超氧阴离子自由基(O₂⁻·)五大经典自由基模型,并结合体外标准化化学检测手段(如电子顺磁共振(ESR)技术),以及细胞层面采用DCFH-DA和DAF‑FMDA荧光探针检测法、组织层面运用DHE荧光探针法,全方位、多层次地评估水凝胶的自由基清除能力与整体抗氧化活性,从而确保表征结果全面且贴合实际生物应用场景。
本期,EFL将为大家解读几种常见的水凝胶抗氧化检测手段,并通过案例分析具体的检测方法、结果解读与科研应用思路。
检测步骤:
1.配制0.1mmol/L左右的DPPH乙醇溶液,避光备用,同时将抗氧化材料剪碎、浸提或直接制备成凝胶悬液,设置空白对照组(无凝胶的纯溶剂)和阳性对照组(常用维生素C、没食子酸);
2.将材料样品液与等体积DPPH溶液充分混合,室温下避光孵育30-60min(时间可根据试验设计调整,保证反应充分);
3.孵育结束后,采用酶标仪测定517nm处的吸光度值,按照公式计算DPPH自由基清除率。
02 ABTS阳离子自由基清除率检测法
检测步骤:
1.将ABTS粉剂与过硫酸钾溶液混合,室温避光孵育12-16h,制备ABTS⁺自由基工作液,使用无水乙醇或PBS稀释至734nm处吸光度约0.7±0.02,保证检测灵敏度;
2.取适量材料浸提液或凝胶分散液,与稀释后的ABTS⁺工作液混合,室温避光反应5-30min(快速反应型抗氧化剂可缩短反应时间);
3.反应结束后立即测定734nm处吸光度,同步设置空白组和阳性对照组,代入公式计算ABTS自由基清除率。
03 PTIO自由基清除率检测法
检测步骤:
1.试剂配制:用pH7.4PBS缓冲液配制0.2mmol/LPTIO自由基工作液,现配现用;将材料剪碎后用PBS浸提24h,离心取上清作为待测样品液;设置空白对照组(PBS替代样品液)、阳性对照组(维生素C或谷胱甘肽溶液),每组3个平行样。
2.样品反应:取等体积PTIO工作液与材料浸提液混合,充分混匀后,置于37℃恒温条件下避光孵育60-90min,保证自由基清除反应充分进行。
3.吸光度检测:孵育结束后,将混合液转移至酶标板,采用酶标仪测定557nm处的吸光度值,记录各组数据。
结果计算:自由基清除率(%)=[1-(样品组吸光度-样品空白吸光度)/(空白对照组吸光度-空白本底吸光度)]×100%

04 羟基自由基(・OH)清除率检测法
核心原理:羟基自由基(・OH)是生物体内活性最强、毒性最大的ROS,可通过Fenton反应(Fe²⁺+H₂O₂)体外生成;亚甲基蓝作为显色探针,与・OH反应发生氧化褪色,在665nm处有特征吸收。各类抗氧化材料(如PDANDs、材料、天然提取物等)中的抗氧化成分可竞争性清除・OH,减少亚甲基蓝氧化,使体系吸光度升高,吸光度越高,清除效果越好。该方法反应快速、特异性强,能模拟生理环境中自由基生成与清除过程,是评估抗氧化材料核心活性的关键指标。
检测步骤:
1.试剂配制:依次配制Fe²⁺溶液(如硫酸亚铁溶液,1mM)、H₂O₂溶液(100mM,避光保存)、亚甲基蓝溶液(0.1mM),建立Fenton反应体系;
2.样品干预:向反应体系中加入系列浓度的抗氧化材料样品液(根据预实验确定有效浓度范围,如12.5-200μg/mL),涡旋混匀后快速反应3-5min(无需额外恒温孵育,避免・OH自发衰减);
3.检测与对照设置:直接测定665nm处吸光度,计算・OH清除率;同步设置空白对照组(无材料)、阳性对照组(经典抗氧化剂如维生素C)、材料空白组(仅材料+溶剂+探针,扣除自身吸光干扰),每组至少3个平行样。
05超氧阴离子自由基(・O₂⁻)清除率检测法
核心原理:超氧阴离子自由基(・O₂⁻)是生物体内ROS的重要前体,参与炎症、损伤等多种病理进程,具有较强氧化性与细胞毒性。体外采用核黄素-甲硫氨酸体系生成・O₂⁻:核黄素在白光照射下以L-甲硫氨酸为电子供体,与氧气反应生成・O₂⁻;硝基四氮唑蓝氯化物(NBT)与・O₂⁻特异性结合生成蓝色甲臜,在560nm处有特征吸收峰。抗氧化材料可通过清除・O₂⁻减少甲臜生成,降低体系吸光度,吸光度越低,・O₂⁻清除能力越强。该方法能模拟炎症微环境下的自由基生成,适配各类材料的针对性抗氧化活性评估。
检测步骤:
1.试剂配制:配制核黄素储备液(10mM,避光保存)、L-甲硫氨酸工作液(10mM,PBS缓冲液pH7.4配制)、NBT工作液(5mM,PBS缓冲液配制,现配现用);抗氧化材料样品液用适配溶剂(超纯水、PBS等)配制系列浓度(12.5-200μg/mL),纳米材料需超声处理10min确保分散均匀;
2.反应体系构建:向离心管或酶标板中依次加入L-甲硫氨酸工作液、核黄素工作液、NBT工作液,再加入等体积材料样品液,涡旋混匀;
3.孵育与检测:将体系置于白光照射下(光照距离10-15cm),室温孵育2h;孵育结束后测定560nm处吸光度,计算・O₂⁻清除率;设置空白对照组、阳性对照组、材料空白组,确保检测条件(光照强度、孵育时间)一致。
结果计算:自由基清除率(%)=[1-(样品组吸光度-样品空白吸光度)/(空白对照组吸光度-空白本底吸光度)]×100%
06细胞内活性氧(ROS)荧光标记法(DCFH-DA荧光探针检测法)
检测步骤:
1.培养L929成纤维细胞、HUVEC内皮细胞或巨噬细胞,采用H₂O₂、脂多糖(LPS)、Rosup等试剂诱导构建细胞氧化应激模型,模拟体内氧化损伤环境;
2.将抗氧化材料浸提液与细胞共培养,再加入DCFH-DA荧光探针孵育20-30min,避光操作避免荧光淬灭;
3.用PBS清洗细胞后,通过荧光显微镜观察细胞内荧光分布,或用流式细胞仪定量检测平均荧光强度,对比空白组、模型组判断抗氧化保护效果。
结果判读:模型组细胞呈现强绿色荧光,抗氧化材料处理组荧光信号显著减弱,说明材料可有效清除细胞内ROS,缓解细胞氧化应激损伤,该方法是连接体外化学检测与体内动物实验的关键桥梁。
07细胞内活性氧(RNS)荧光标记法(DAF-FMDA荧光探针检测法)
检测步骤:
1.细胞培养与模型构建:培养L929成纤维细胞、HUVEC内皮细胞或巨噬细胞,采用脂多糖(LPS)诱导细胞产生大量NO,构建亚硝化应激细胞模型,模拟体内炎症微环境下的NO过量生成状态;
2.样品共培养与探针孵育:将抗氧化材料浸提液与NO应激模型细胞共培养一定时间(通常24h),随后加入DAF-FMDA荧光探针,37℃、5%CO₂培养箱中避光孵育20-30min,确保探针充分进入细胞并完成活化;
3.清洗与检测:用预温的PBS缓冲液轻轻清洗细胞3次,去除未进入细胞的游离探针,避免荧光干扰;通过荧光显微镜观察细胞内荧光分布、拍照记录,或用流式细胞仪定量检测细胞平均荧光强度,同步设置正常细胞组、NO应激模型组、样品处理组、阳性对照组(如L-精氨酸抑制剂)。
结果判读:NO应激模型组细胞呈现强绿色荧光,表明细胞内NO含量较高;抗氧化材料处理组细胞荧光信号显著减弱,荧光强度越低,说明材料清除细胞内NO、缓解亚硝化应激的能力越强;结合荧光图片的荧光分布均匀度,可进一步判断材料对细胞内NO的清除效果,为材料抗炎抗氧化机制研究提供细胞层面的直接证据。
08 DHE荧光探针法组织内活性氧(ROS)荧光标记法
检测步骤:
1.动物模型构建与样品处理:根据研究目标构建相应病理模型(如炎症模型、损伤模型、衰老模型等),选取目标检测组织(如肠道、肝脏、肾脏、皮肤、肺组织等);将实验动物分为正常对照组、病理模型组、抗氧化材料处理组、阳性对照组(如临床抗氧化药物),按实验设计完成给药或干预后,处死动物并快速分离目标组织。
2.组织切片制备:将新鲜目标组织用生理盐水冲洗干净,去除组织表面残留的血液、分泌物或内容物,避免杂质干扰;液氮速冻后置于-80℃保存,或直接进行冷冻切片;用冷冻切片机将组织切成5-10μm厚的冷冻切片,贴附于多聚赖氨酸包被的载玻片上,室温晾干备用(避免组织脱落)。
3.探针孵育与清洗:向组织切片上均匀滴加终浓度8-10μM的DHE荧光探针工作液,确保探针完全覆盖组织切片;将载玻片放入湿盒中,37℃避光孵育30-45min(根据组织类型调整,致密组织可延长至60min),确保探针充分进入组织细胞并完成氧化活化;孵育结束后,用预温至37℃的PBS缓冲液轻轻清洗切片3次(每次5min),去除未进入细胞的游离探针,避免荧光干扰。
4.复染与检测:滴加DAPI染液(终浓度1μg/mL),室温避光孵育10min,对细胞核进行复染,便于定位组织细胞结构;PBS清洗2次后,用抗荧光淬灭剂封片;通过荧光显微镜观察组织内红色荧光分布与强度,拍照记录(随机选取3-5个不同视野,确保覆盖组织关键区域);用ImageJ软件定量分析平均荧光密度值(OD值)或荧光面积占比,量化组织内ROS水平。
结果判读:正常对照组组织仅呈现微弱红色荧光,表明生理状态下ROS含量低;病理模型组组织呈现强红色荧光,且荧光分布与病理损伤区域高度重合,提示病变组织内ROS大量积累;抗氧化材料处理组组织的红色荧光信号显著减弱,荧光强度接近正常对照组,说明材料能高效清除病变组织内的过量ROS,缓解氧化应激损伤。通过对比材料处理组与对照组(如未修饰材料、临床药物)的荧光强度,可验证材料的抗氧化优势;结合组织病理染色(如H&E染色),能进一步关联ROS清除效果与组织损伤修复程度,为材料在体抗氧化治疗机制提供直接的组织层面证据。
09 活性氧(ROS)/活性氮(RNS)电子顺磁共振(ESR)检测法
核心原理:ESR(电子顺磁共振)技术基于未成对电子的磁共振特性,是自由基直接定性与定量检测的金标准。自由基作为含未成对电子的活性物质,在静磁场中会发生能级分裂,施加特定频率微波辐射时,电子在能级间跃迁产生共振信号,信号强度与自由基浓度呈正相关。实验选用5,5-二甲基-1-吡咯啉N-氧化物(DMPO)、α-苯基-N-叔丁基硝酮(PBN)等特异性捕获剂,与短寿命自由基快速结合形成稳定自旋加合物,延长检测窗口。通过对比加入抗氧化材料前后的ESR共振信号强度,可直接量化材料的自由基清除效率,为其广谱抗氧化活性提供分子层面直接证据,补充紫外-可见光谱法、荧光探针法等间接检测的可靠性,适配各类抗氧化材料的核心性能表征。
检测步骤:
1.试剂配制与体系构建:
配制系列自由基发生体系:・OH由H₂O₂与Fe²⁺通过Fenton反应生成,・O₂⁻由核黄素与L-甲硫氨酸在白光照射下生成,DPPH・、ABTS⁺・直接用无水乙醇或缓冲液溶解配制;
配制捕获剂溶液:DMPO终浓度50-100mM(适配・OH、・O₂⁻检测),PBN终浓度10-20mM(适配脂溶性自由基检测);
配制抗氧化材料样品溶液:根据材料特性,用超纯水、PBS缓冲液或无水乙醇配制系列浓度(0.1-200μg/mL),确保材料充分分散或溶解,避免团聚。
2.样品与自由基体系共孵育:按比例将抗氧化材料样品溶液与自由基发生体系混合,涡旋振荡10-15s混匀;立即加入捕获剂,快速颠倒混匀后,迅速转移至ESR石英毛细管中(避免气泡产生);设置空白对照组(仅含溶剂与捕获剂)、自由基模型组(不含材料的自由基体系+捕获剂)、阳性对照组(经典抗氧化剂如维生素C、谷胱甘肽+自由基体系+捕获剂),每组设置3个平行样。
3.ESR信号检测:将石英毛细管放入ESR光谱仪样品腔,设定统一检测参数:微波功率10-20mW、中心磁场3400-3500G、扫描范围100-200G、扫描时间3-5min、调制幅度0.5-1G;启动仪器采集信号,记录各组ESR共振谱图、峰高及峰面积数据。
4.数据处理与分析:
用ESR光谱分析软件读取各组共振峰特征参数(峰高、峰面积);以自由基模型组信号强度为基准,计算不同浓度抗氧化材料对目标自由基的清除率(清除率=(模型组信号强度-样品组信号强度)/模型组信号强度×100%);绘制浓度-清除率曲线,明确材料抗氧化活性的浓度依赖性,计算半数清除浓度(EC50)以量化抗氧化能力。
结果判读:自由基模型组会出现特征性ESR共振峰(・OH-DMPO加合物呈4重对称峰,・O₂⁻-DMPO加合物呈6重峰,DPPH・呈单一尖锐峰),且信号强度高,表明体系中自由基含量丰富;加入抗氧化材料后,共振峰的峰高与峰面积显著降低,降低幅度随材料浓度升高而增大,说明材料能有效捕获或清除目标自由基。
案例一:Advanced Science(IF=14.1)聚多巴胺纳米点通过恢复氧化还原稳态改善炎症性肠病2025.08.23
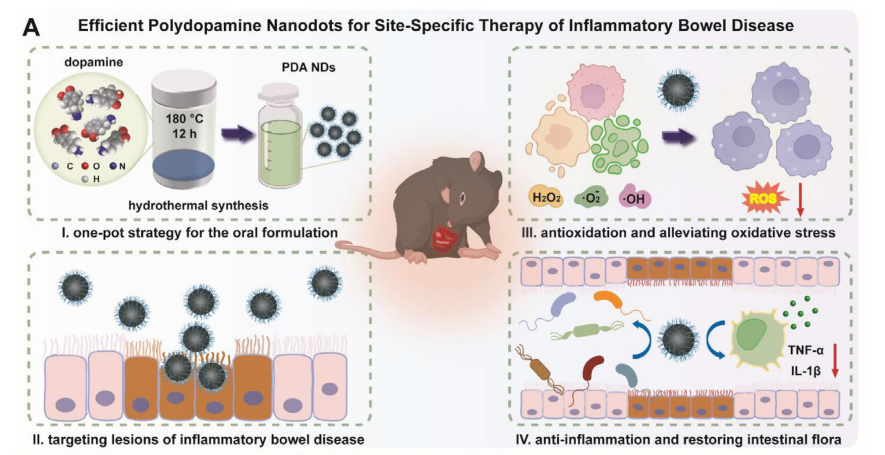
简介:该研究设计制备聚多巴胺纳米点(PDANDs),凭借其本征广谱自由基清除活性,高效清除肠道过量活性氧(ROS)与活性氮(RNS),恢复氧化还原平衡,实现炎症性肠病靶向抗氧化治疗。
参考资料:
https://doi.org/10.1002/advs.202508674
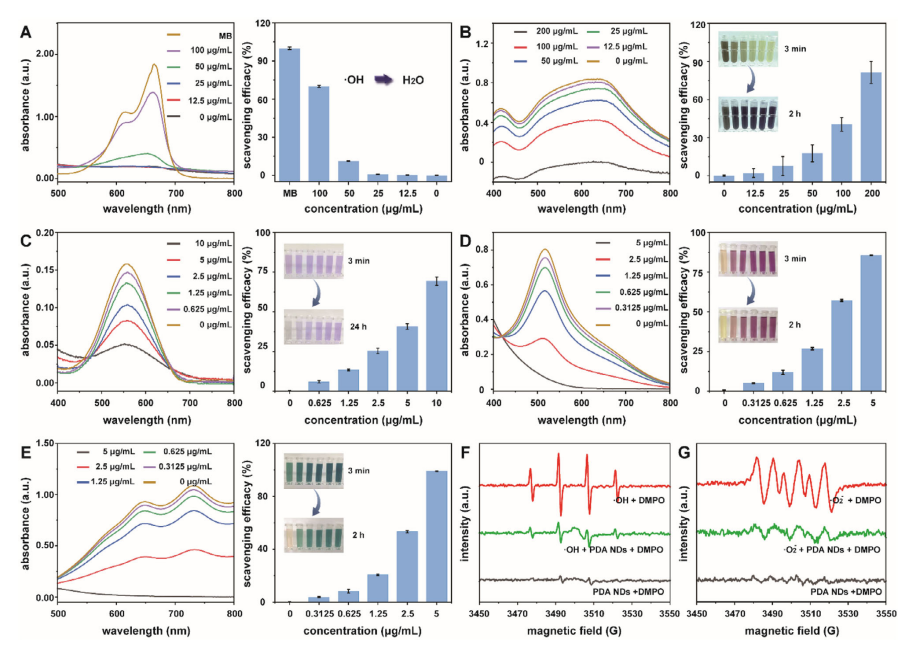
图1 聚多巴胺纳米点(PDANDs)的抗氧化性能表征
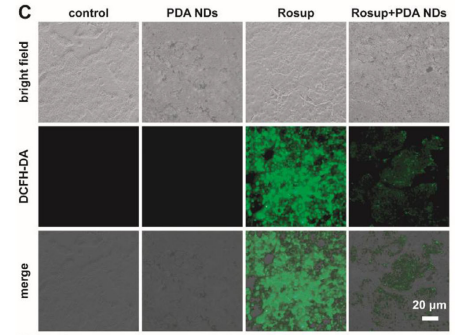
图2 经不同处理后的Caco-2细胞的DCFH-DA荧光图像
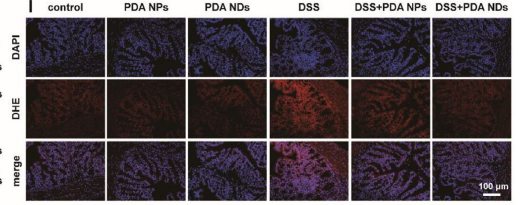
图3 以DHE作为荧光探针不同结肠组织样本中活性氧(ROS)的荧光图像
检测手段:DPPH自由基清除法、ABTS自由基清除法、羟基自由基(・OH)清除法、超氧阴离子(・O₂⁻)清除法、PTIO・清除法、DCFH‑DA荧光探针法、DHE荧光探针法、ESR电子顺磁共振法
检测结果:
(1)研究者以DPPH、ABTS、・OH、・O₂⁻、PTIO・为自由基模型,结果显示PDANDs呈浓度依赖性高效清除各类ROS/RNS,100μg/mL可清除超70%羟基自由基,抗氧化能力显著优于传统PDA纳米颗粒。
(2)ESR结果直接证实,PDANDs可显著降低DMPO-・OH与DMPO-・O₂⁻特征信号,直接淬灭短寿命高活性氧自由基。
(3)细胞与组织水平采用DCFH‑DA与DHE探针检测,Rosup诱导后Caco-2细胞内ROS显著升高,PDANDs处理后绿色/红色荧光强度显著下。
案例二:Journal of Nanobiotechnology(IF=12.6)碳点纳米酶材料调控氧化应激促进牙髓炎牙髓再生2024.09.04
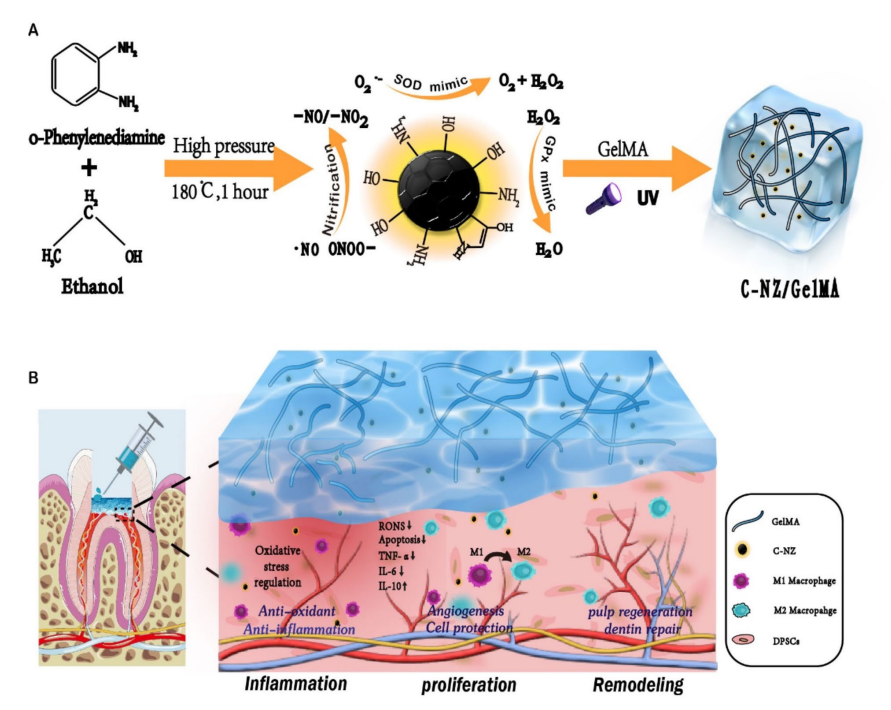
简介:该研究将氮掺杂碳点纳米酶(C‑NZ)载入可注射光固化GelMA材料中,构建C‑NZ/GelMA抗氧化体系,依托碳点纳米酶的高效自由基清除能力,实现对活性氧(ROS)和活性氮(RNS)的同步清除,改善牙髓炎氧化应激微环境。
参考资料:
https://doi.org/10.1186/s12951-024-02810-z
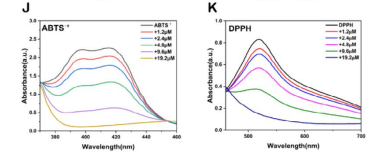
图4 ABTS•+水溶液以及DPPH溶液在添加不同浓度C-NZ条件下的吸收光谱
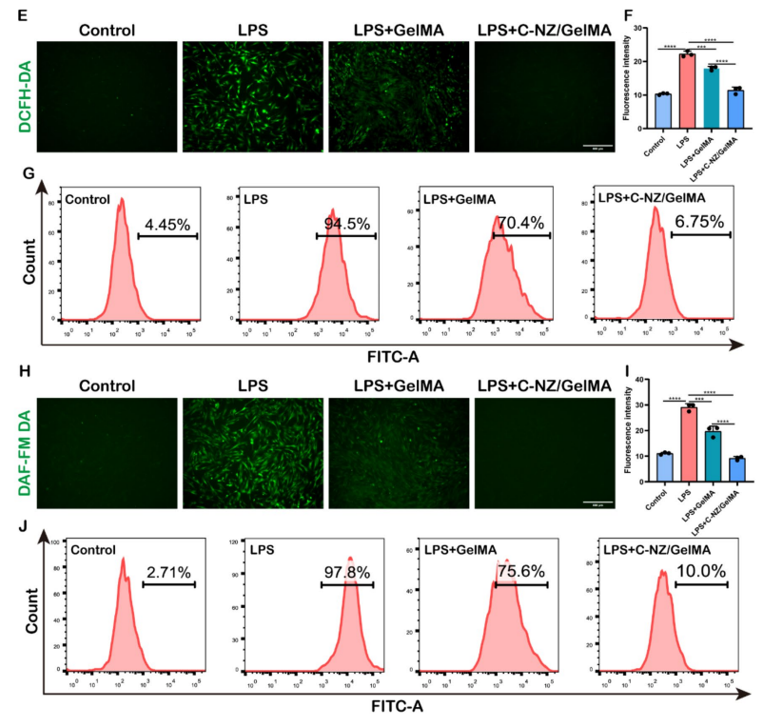
图5 C-NZ/GelMA材料在抗氧化方面的作用
检测手段:ABTS自由基清除法、DPPH自由基清除法、DCFH‑DA荧光探针法、DAF‑FMDA荧光探针法
检测结果:
(1)研究者以ABTS、DPPH自由基为体外评估模型,测试C‑NZ/GelMA材料的总抗氧化能力,结果显示C‑NZ/GelMA材料可高效清除ABTS与DPPH自由基,且清除效果呈浓度依赖性,显著优于纯GelMA材料,证明碳点纳米酶赋予材料优异的体外抗氧化性能。
(2)采用DCFH‑DA荧光探针检测Pg‑LPS诱导的人牙髓干细胞内总ROS水平,荧光图像与定量分析表明,C‑NZ/GelMA材料可显著降低细胞内绿色荧光强度,将高表达的ROS恢复至接近正常水平,有效缓解细胞氧化损伤。
(3)利用DAF‑FMDA荧光探针检测细胞内活性氮(・NO)水平,结果显示C‑NZ/GelMA材料可明显减弱荧光信号,高效清除炎症微环境中过量的・NO,同步实现ROS与RNS的双重清除,为牙髓细胞提供保护。
案例三:Advanced Functional Materials(IF=19)负载石榴皮单宁的细胞膜囊泡生物墨水用于抗氧化与软骨再生修复2025.05.25
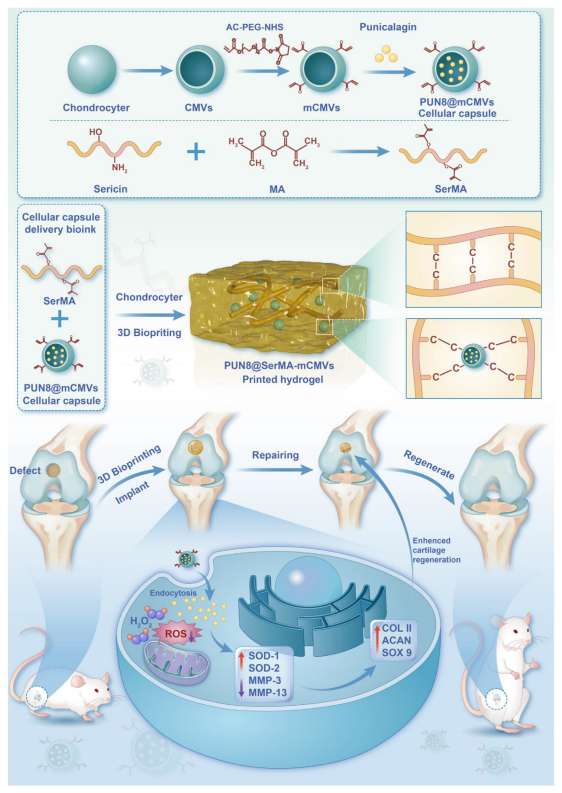
简介:该研究将负载石榴皮单宁(PUN)的软骨细胞膜囊泡(CMVs)与甲基丙烯酰化丝胶蛋白(SerMA)结合,构建PUN@SerMA‑mCMV生物墨水,依托石榴皮单宁的多羟基结构,实现高效清除活性氧(ROS),为软骨修复提供抗氧化微环境。
参考资料:
https://doi.org/10.1002/adfm.202504180
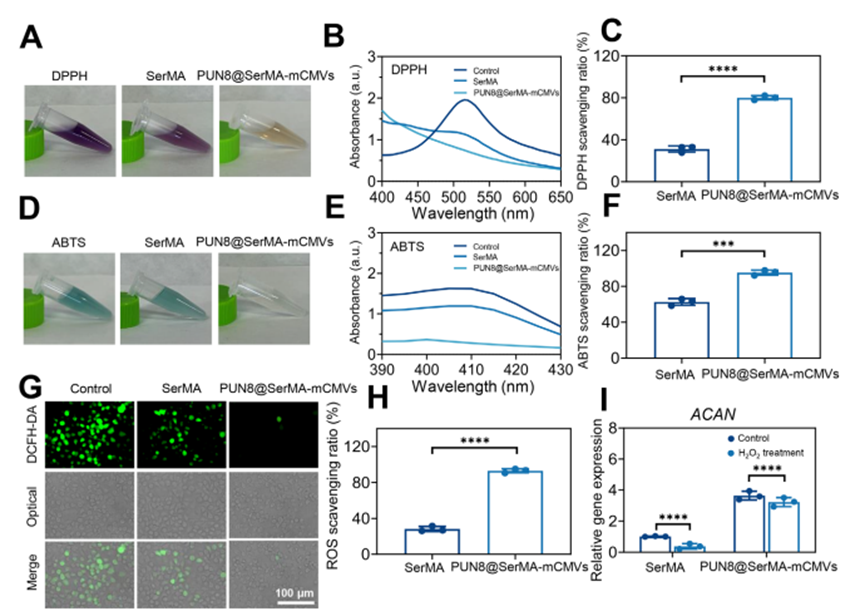
图6 PUN@SerMA‑mCMV生物墨水的抗氧化性能表征
检测手段:
DPPH自由基清除法、ABTS自由基清除法、DCFH‑DA荧光探针法
检测结果:
(1)研究者以DPPH、ABTS自由基为体外评估模型,测试PUN@SerMA‑mCMV材料的自由基清除能力,结果显示该材料对DPPH自由基清除率约79.82%,对ABTS自由基清除率高达94.28%,显著高于纯SerMA材料,证明石榴皮单宁赋予生物墨水优异的总抗氧化能力。
(2)采用DCFH‑DA荧光探针检测H₂O₂诱导的软骨细胞内ROS水平,荧光图像显示PUN@SerMA‑mCMV材料可显著降低细胞内绿色荧光强度,ROS清除率达93.0%,有效缓解细胞氧化应激损伤。
EFL小贴士:
通过对以上9种常见抗氧化检测手段的学习,研究者可从体外化学层面、细胞层面、组织层面及分子层面综合分析抗氧化材料的抗氧化性能。其中,不同检测手段各有优势与适配场景:ESR检测法作为自由基直接定性定量的“金标准”,可精准捕获・OH、・O₂⁻等短寿命自由基,结果可信度最高;DCFH-DA、DAF-FM DA、DHE三种荧光探针法分别实现细胞内ROS、RNS及组织内ROS的可视化检测,能直观呈现材料在生物体内的抗氧化效果;DPPH、ABTS、PTIO、・OH、・O₂⁻五种体外化学检测法操作简便、成本较低,适合抗氧化材料的高通量筛选与初步活性评估。研究者可根据实验需求(如材料筛选阶段、机制验证阶段)、检测对象(自由基类型、样本类型)及精度要求,组合多种检测方法(如体外化学法+细胞/组织荧光法+ESR验证),全面、系统地表征材料的广谱抗氧化活性,确保实验结果的科学性与可靠性。